樫村吉晃 古川一暁
機能物質科学研究部
生体膜の基本構造である脂質二分子膜は、固体基板上に自己組織化により自発的に形成させることができる。我々はこの人工細胞膜の自発展開特性を利用して、ナノギャップ構造が脂質分子や膜に埋め込んだ分子の運動性に及ぼす影響について調べてきた[1、2]。本研究では、ナノギャップ構造を電極として利用し、ここに印加した電圧が自発展開挙動に及ぼす影響を検討した[3]。
卵黄由来の脂質Egg-PCとEgg-PGの混合物(モル比7:3)に、色素結合脂質Texas Red-DHPEを1 mol%添加した。SiO2基板上に幅10 µmの流路とその両端に脂質の収容部を作製した。流路内にナノギャップ電極を備え、電極間に直流電圧を印加した。収容部の一端に試料を付着させ、0.1-100 mM NaClを含む緩衝液中に浸漬させ自発展開の時間発展を観察した。
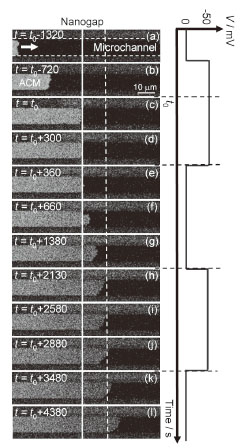
図1は流路に沿って自発展開する人工細胞膜の蛍光顕微鏡像である(電解質100 mM NaCl, ナノギャップ幅5 nm)。ナノギャップ通過前は電圧印加による影響は見られなかったが[図1(a)、(b)]、膜の先端がナノギャップに到達すると、電圧印加時に自発展開が停止する挙動が観測された[図1(c)、(d)]。印加電圧を0
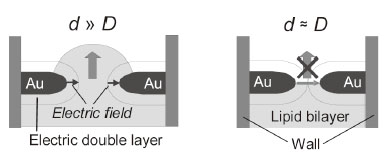
Vとすると膜は自発展開を再開した[図1(e)-(g)]。この自発展開の停止/進行の挙動は、印加電圧のON/OFFによって繰り返し観測された[図1(h)-(l)]。この振る舞いには、ナノギャップ間における電気二重層(電解質濃度に依存)の存在が重要な寄与をしていることが、電気ポテンシャル計算や電解質濃度依存性の実験から明らかになった。すなわち、マクロなスケールでは電解質溶液中における電場は対イオンの効果により打ち消されてしまうが、ギャップの幅(d )が電気二重層の厚さ(D )と同程度まで小さくなると(100 mM NaCl水溶液でD 〜 1 nm)、ナノギャップ間に有効な電場が形成される。この強い電場により脂質分子がナノギャップ間に静電トラップされ、分子の供給がなくなるために自発展開が停止する(図2)[3]。これはナノギャップを分子ゲートとして用いた初めての例であり、ナノバイオデバイスの要素技術として大きな期待が持たれる。
本研究は科研費の援助を受けて行われた。
[1] Y. Kashimura et al., Jpn. J. Appl. Phys. 47 (2008) 3248.
[2] Y. Kashimura et al., Jpn. J. Appl. Phys. 49 (2010) 04DL15.
[3] Y. Kashimura et al., J. Am. Chem. Soc. 133 (2011) 6118.
 |
 |
|||||
|
|