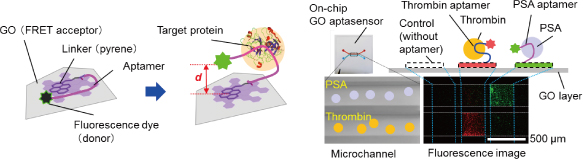
グラフェンおよびそれらの誘導体表面では、表面に近接した分子との相互作用に応じたエネルギー移動反応が生じる。このエネルギー移動反応を、生体分子に特異的な反応と組み合わせて可視化すれば、バイオセンサなどの生体分子インターフェースを構築することができる。私たちは、固体表面に固定した酸化グラフェン(Graphene Oxide, GO)を用いて、タンパク質を選択的かつ高感度に検出するGOアプタセンサの構築に成功した(図1左)[1]。さらに、表面に固定化されているという特長を活かして、マイクロ流路を搭載したオンチップ型GOアプタセンサを実現し、これが複数の異なる検体に対する応答の定量比較や濃度依存測定において威力を発揮することを示した[2, 3]。
生体分子認識に用いる核酸アプタマ(特定の分子に選択吸着する1本鎖DNA/RNA)は、種々の環境下で安定な物質であり、適用できる標的分子の種類の多様性にも優れる。種々の標的分子に対応するアプタマを用いて、血液凝固に関与するタンパク質であるトロンビン、前立腺特異抗原(PSA)、インフルエンザウイルス外被糖タンパク質(ヘマグルチニン)の検出に成功し、センサの汎用性を確認した。このうち、トロンビンとPSAの2種類のアプタマを同一チップ上にアレイ化し、多成分同時検出に成功した(図1右)[3]。また、分子認識機能を損なうことなく、自由自在な分子設計による機能化が可能であることも、アプタマの大きな魅力である。これにより、所望の機能を有する様々な分子プローブの創生が実現できる。これまでに、分子設計によりオンチップ型GOアプタセンサの高感度化に成功し、マイクロデバイス技術を用いた定量的な比較実験から、その効果を実証した[2]。