人工細胞膜自発展開の静電制御
樫村![]() 晃 古川一暁
晃 古川一暁
機能物質科学研究部
我々は固体表面に作製した人工細胞膜(脂質二分子膜)の時間的・空間的な成長制御を目的とし、ナノギャップを通過する人工細胞膜に電圧を印加・開放することによって自発展開の停止/進行を制御可能なことを見出し、その動作モデルを提案してきた[1]。本研究では、電気二重層の精密チューニングという観点から、様々な電解質濃度、ナノギャップで自発展開の制御実験を行い、モデルの妥当性を検討した[2]。
卵黄由来の電気的中性のL-α-PCとアニオン性のL-α-PGの混合脂質(モル比7:3)に色素結合脂質Texas Red-DHPEを1 mol%混合した。SiO2基板上に幅10 µmの流路とその両端に収容部を作製し、流路内にはナノギャップ電極を備えた。収容部の一端に脂質試料を付着させ、電極間に直流電圧(-50
mV)を印加しながら、電解質溶液中(1-100 mM NaCl)に浸漬させて自発展開を開始し、その時間発展を観察した。
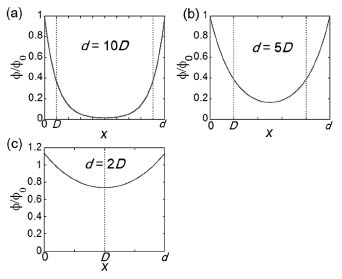
ナノスケールの領域では、電圧印加の効果はナノギャップの幅(d) と電気二重層の厚さ(D) との相対比に依存する。図1は代表的なケースについて、ナノギャップ電極間の電気ポテンシャルを計算した結果である。d ![]() Dの場合(a)、電場は電気二重層の外側では対イオンによって遮蔽されてしまい、ナノギャップ表面近傍でしか有効ではない。すなわち、人工細胞膜が通過可能なチャネルが存在する。一方、d
Dの場合(a)、電場は電気二重層の外側では対イオンによって遮蔽されてしまい、ナノギャップ表面近傍でしか有効ではない。すなわち、人工細胞膜が通過可能なチャネルが存在する。一方、d ![]() Dの場合(b, c)にはナノギャップ両端からの電気二重層同士が重なりをもつようになり、ナノギャップ全体に渡って有効な電場が生じる。この状況では、強い電場によりナノギャップ間に脂質分子が静電トラップされ、自発展開膜への分子の供給がなくなるために成長が停止する。図2は電解質濃度を変えて、自発展開の停止/進行制御に対する影響を調べた結果である。電気二重層の厚さは電解質濃度(c)に依存し、NaCl水溶液の場合はD
〜 0.304/
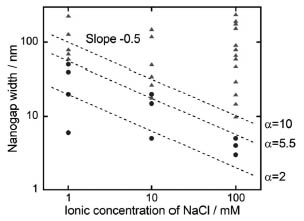
Dの場合(b, c)にはナノギャップ両端からの電気二重層同士が重なりをもつようになり、ナノギャップ全体に渡って有効な電場が生じる。この状況では、強い電場によりナノギャップ間に脂質分子が静電トラップされ、自発展開膜への分子の供給がなくなるために成長が停止する。図2は電解質濃度を変えて、自発展開の停止/進行制御に対する影響を調べた結果である。電気二重層の厚さは電解質濃度(c)に依存し、NaCl水溶液の場合はD
〜 0.304/![]() で与えられる。NaCl濃度が100 mM (D 〜 1 nm)のときは、ナノギャップの幅が5 nm以下の条件でのみ電圧による成長制御が可能であったが、1
mM (D 〜 10 nm) ではナノギャップの幅が一桁大きい50 nmでも制御することが可能であった。各濃度において、いずれもd 〜 5.5Dが電場制御可能か否かの閾値であることがわかった。この結果は電気ポテンシャル計算の結果(d 〜 5D)ともよく一致し、提案モデルの妥当性を実証することができた。
で与えられる。NaCl濃度が100 mM (D 〜 1 nm)のときは、ナノギャップの幅が5 nm以下の条件でのみ電圧による成長制御が可能であったが、1
mM (D 〜 10 nm) ではナノギャップの幅が一桁大きい50 nmでも制御することが可能であった。各濃度において、いずれもd 〜 5.5Dが電場制御可能か否かの閾値であることがわかった。この結果は電気ポテンシャル計算の結果(d 〜 5D)ともよく一致し、提案モデルの妥当性を実証することができた。
[1] Y. Kashimura et al., J. Am. Chem. Soc. 133 (2011) 6118.
[2] Y. Kashimura et al., IEICE TRANS. ELECTRON 96-C (2013) 344.
 |
 |
||||
|
|